Eines von 500 Kindern wird mit einem Hörschaden geboren, in 50 bis 70 Prozent der Fälle ist ein Gendefekt die Ursache. Das Deutsche Primatenzentrum – Leibniz-Institut für Primatenforschung, die Universitätsmedizin Göttingen und das Max-Planck-Institut für experimentelle Medizin wollen in einem gemeinsamen Forschungsprojekt eine Gentherapie etablieren, mit der erblich bedingte Gehörlosigkeit behandelt werden kann. Die Methode soll an Weißbüschelaffen entwickelt und dann auf menschliche Patienten übertragen werden. Die Leibniz-Gemeinschaft hat jetzt die Förderung über rund eine Million Euro zugesagt.
Otoferlin ist ein Protein, das in den Haarzellen des Innenohrs vorkommt. Wenn das Gen, das den Bauplan für Otoferlin enthält, defekt ist, wird kein funktionsfähiges Protein gebildet und der betroffene Mensch ist gehörlos. Für das zugrundeliegende Gen (OTOF) sind hunderte krankmachende Mutationen beschrieben, die für bis zu 10 Prozent der vererbten Schwerhörigkeit verantwortlich sind. Da eine genetische Wiederherstellung der Otoferlinfunktion auch nach der Entwicklung des Ohrs möglich ist, zählt dieses Gen zu den vielversprechendsten Angriffspunkten zukünftiger Gentherapien. Auf dem Weg zur klinischen Anwendung will ein Team um den Stammzell- und Entwicklungsbiologen Rüdiger Behr vom Deutschen Primatenzentrum sowie den Neurowissenschaftler und Mediziner Tobias Moser von der Universitätsmedizin Göttingen diesen Ansatz nun in Weißbüschelaffen anwenden.
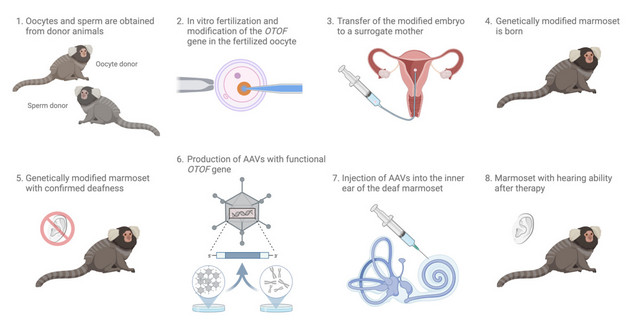
Um die Funktion der Gentherapie untersuchen zu können, benötigen die Forscher Versuchstiere, die genetisch so modifiziert wurden, dass sie aufgrund eines Defekts im OTOF-Gen gehörlos sind. Da diese Tiere taub geboren werden, machen sie nie die Erfahrung, dass sie den Gehörsinn verlieren. Diese genetischen Verfahren sind schmerzfrei für die Tiere. Bei Mäusen ist es bereits gelungen, taub geborene Tiere zu züchten. Dies ist bei Mäusen bereits gelungen. Behr und sein Team wollen die Methode jetzt auf eine Tierart übertragen, die dem Menschen neurophysiologisch, immunologisch und genetisch möglichst ähnlich ist, um so eine besonders gute Übertragbarkeit der Forschungsergebnisse auf den Menschen zu erreichen. „Wir setzen Weißbüschelaffen ein, da ihr Hörsystem dem menschlichen sehr ähnlich ist und sie aufgrund ihres ausgeprägten Kommunikationsverhaltens für Hörstudien besonders gut geeignet sind“, sagt Marcus Jeschke, der bereits seit Jahren an Weißbüschelaffen forscht.
Im nächsten Schritt soll der so erzeugte Gendefekt repariert werden. Dazu werden adenoassoziierte Viren (AAV) verwendet. AAVs dienen als Genfähren, sie können mit Erbinformationen befüllt werden und diese dann in Körperzellen einschleusen, ohne den Organismus zu schädigen. Die mit einem funktionierenden OTOF-Gen bestückten AAVs sollen ins Innenohr der tauben Weißbüschelaffen gespritzt werden.
„Eine große Herausforderung ist dabei, geeignete adenoassoziierte Viren zu finden, die spezifisch und langanhaltend Haarzellen im Innenohr genetisch verändern.“ sagt Kathrin Kusch, die sich am Deutschen Primatenzentrum auf AAVs spezialisiert hat. Dass diese Methode prinzipiell funktioniert, wurde unter anderem von Tobias Mosers Team bereits an Mäusen gezeigt. Allerdings ist noch unklar, wie lange der Effekt anhält und welche Dosis an Viren in größeren Tiermodellen eingesetzt werden muss. „Diese Fragen müssen wir beantworten, bevor die Therapie klinisch geprüft werden kann“, sagt Tobias Moser.
„Sollte die Methode so funktionieren, wie wir es vermuten, so wäre sie eine Blaupause für andere Krankheiten, die mittels Gentherapie behandelt werden können. Dazu zählen Defekte in der Netzhaut oder auch im Herzmuskel“, blickt Rüdiger Behr in die Zukunft.
Kontakt
Prof. Dr. Rüdiger Behr
+49 551 3851-132
Prof. Dr. Tobias Moser
+49 551 3851-321
Dr. Susanne Diederich
+49 551 3851-359